研究揭示药物载体高效递释的物理药剂学新机制
| 来源: 【字号:大 中 小】
5月21日,中国科学院上海药物研究所研究员甘勇与国家纳米科学中心研究员施兴华合作,在《美国国家科学院院刊》(PNAS)上在线发表了题为Curvature-mediated Rapid Extravasation and Penetration of Nanoparticles against Interstitial Fluid Pressure for Improved Drug Delivery的研究论文。该研究为设计高效递释的药物载体以克服体内复杂屏障提供了全新思路。
药物载体可精准调控活性分子如小分子、多肽、蛋白质和核酸等在体内的时间和空间分布,在改善药物的安全性和有效性方面发挥重要作用。然而,载体在真实生物体内往往面临着复杂的生理和病理屏障,限制了递药效率。在抵达靶位之前,载体需要“翻山越岭”地克服酶屏障、血液循环屏障、组织渗透屏障、细胞屏障及胞内转运屏障等。这些屏障限制了药物载体的输送过程,使得到达靶组织内的药物仅有不到0.7%。为了应对这些挑战,研究药物载体与生物屏障之间的相互作用至关重要。近年来的研究表明,载体的物理属性如形状、刚度、尺度和表面性质,是决定其与生物屏障相互作用的关键因素,有望通过调控载体的物理属性而提高药物的安全性和有效性。
该团队独立设计并合成了多种不同形状的药物载体,并通过透射电子显微镜等技术进行了表征。实验发现,与球形、椭球形及棒形载体相比,尖锐梭形的纳米载体(ENP5)在体内外高间质压环境中展现出更优异的外渗和内渗能力。该研究在小鼠模型中评价了负载化疗药物阿霉素(Dox)的不同形状载体的抗肿瘤药效。与对照组相比,Dox@ENP5对肿瘤的抑制增强,其肿瘤抑制率高于90%,并延长HCC肝癌小鼠的生存周期。
进一步,结合超高分辨率显微镜观测和分子模拟技术,该团队探讨了载体克服高间质压屏障的三维运动模式及其力学机制。研究发现,在血管外渗过程中,载体的高曲率有助于减少压力梯度产生的流体阻力,加速了梭形载体的迁移速度;在组织内渗过程中,高曲率通过促进载体的旋转运动,增加了其在高压密集的细胞外基质中的跳跃频率,加速了载体向肿瘤深层的穿透,提升了药物的递送效率。
研究工作得到国家自然科学基金委员会和中国科学院等的支持。
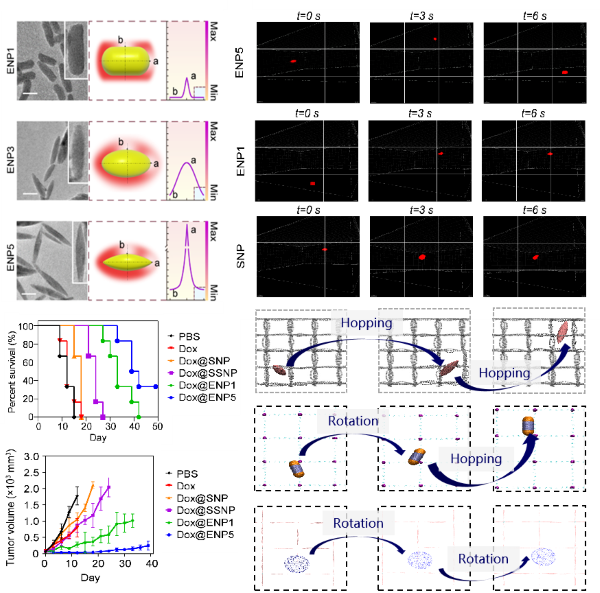
曲率介导载体高效输运的效果及微观机制
